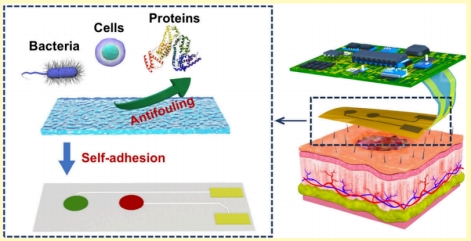
为应对创面感染早期识别与动态管理的临床需求,康复大学江天甲团队与合作团队提出以“自粘附两性离子水凝胶薄层”赋能可穿戴电位型离子传感芯片的通用抗生物污染策略:采用多巴胺(Dopamine)触发的一步凝胶化合成PSBMA-DA-PEGDA自粘附水凝胶,在无需额外表面改性的条件下,使其在柔性芯片的H⁺选择性电极、共享参比电极及PI基底表面形成致密、低溶胀、强湿黏附涂层,显著抑制细菌、蛋白与细胞黏附,并降低聚合物膜电极的细胞毒性。器件层面构建NiCo₂S₄固接全固态H⁺-ISE与PVB/PU保护参比体系,在保证近Nernst斜率与快速响应的同时,获得良好的机械柔性(弯折至180°与多循环不降敏)、可逆稳定与14天贮存稳定;在模拟创面液(SWF)中保持线性与选择性,对Ca²⁺与乳酸等干扰具耐受。更重要的是,通过设计多通道柔性pH电极阵列,实现对大面积创面的时间—空间分辨pH成像:在大鼠感染模型中,术后第3天感染创面呈碱性上移(pH≈8.1),经治疗后第7天回落至接近生理水平,创缘高pH区域显著收缩,验证了在体原位监测与疗效评估的可行性。上述优异性能源自材料/器件的协同设计:两性离子聚合物强水合层与低溶胀抑制生物污染并降低离子传质阻力;多巴胺引发的共价/非共价(氢键、静电、π-π等)多重网络赋予涂层强湿黏附与高延展;NiCo₂S₄提供稳定离子-电子传递界面。该策略可普适扩展至与创面直接接触的各类可穿戴电极系统,有望推广至多离子/代谢物体征的原位监测。相关论文以“A Biocompatible Wearable Potentiometric Sensing Chip for in Situ Wound Monitoring”为题,发表在ACS Sens.上。
DOI:10.1021/acssensors.5c03506
